
Les richesses du désert
Alan Williams, Chimiste, Prof.hon. université de Genève
Mars 2025
Le désert d’Atacama, qui comprend l’extrême nord du Chili ainsi que les régions avoisinantes du Pérou et de la Bolivie, est une des régions les plus arides du monde. Il se trouve autour de la latitude de 22° S où les cellules atmosphériques de Hadley et de Ferrel se rencontrent, donnant lieu à un courant descendant d’air sec. C’est ainsi que plusieurs zones désertiques du monde se trouvent aux latitudes ± 20° (voir texte ‘Une goutte dans l’océan’). Dans le cas du désert d’Atacama, l’aridité est augmentée par la présence de deux chaînes de montagne, les Andes à l’est et la Cordillère de la Côte à l’ouest, qui, chacune, protège la région de l’arrivée de vents humides venant, respectivement, de l’Atlantique et du Pacifique. En conséquence, certaines stations météorologiques de la région n’ont pas enregistré de pluie en 50 ans. Ces conditions sont propices à la formation de minéraux par l’évaporation des solutions aqueuses.

Déposition de sel à la suite de l’évaporation de l’eau d’un lac dans le désert d’Atacama. Photo Barbara Courvoisier.
La pluviométrie est très faible mais non nulle. Le fort ensoleillement favorise l’évaporation du peu d’eau qui tombe avant qu’elle ne puisse couler dans l’océan. Or, cette eau n’est pas pure mais contient des sels qui ont été lessivés des roches ou qui proviennent des sources liées à l’activité volcanique de la chaîne des Andes. Ces conditions sont favorables à la formation des évaporites, des roches formées par l’évaporation de l’eau de ces solutions salées. Les plus connus de ces évaporites sont sans doute les dépôts de chlorure de sodium (ou sel commun) formés lors de l’évaporation de l’eau de mer. Toutefois, le chlorure de sodium n’est de loin pas la seule substance trouvée comme évaporite. De manière générale, les sels se déposent en ordre inverse de leur solubilité : carbonate de calcium (calcite), puis sulfate de calcium (gypse ou anhydrite), puis chlorure de sodium (halite), suivi d’autres sels plus solubles dont des sels de magnésium et de potassium. La particularité du désert d’Atacama est la présence de dépôts comprenant d’important quantités du nitrate de sodium (aussi connu sous le nom de nitratine ou nitronatrite).
Le salpêtre du Chili
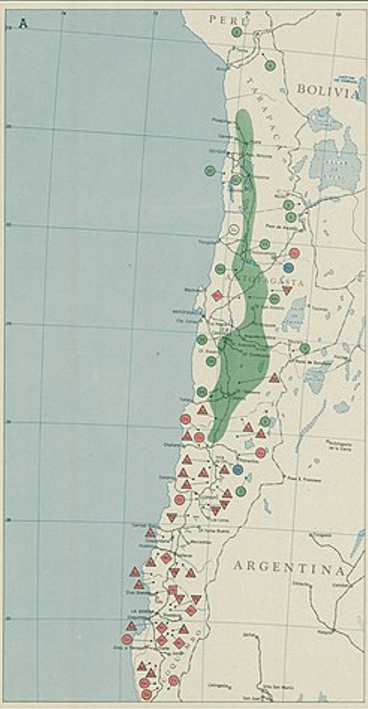
Le nitrate de sodium est très soluble et devrait donc être parmi les derniers sels à se déposer. Il est trouvé dans des dépôts appelés caliche. Au Chili le caliche se compose d’un mélange de gypse, chlorure de sodium, nitrate de sodium (aussi appelé salitre) qui forme un solide avec du sable et du gravier. Une composition typique est 7,5% de nitrate de sodium, 19% de sulfate de sodium, 5% de chlorure de sodium, le reste étant des roches insolubles, mais elle varie beaucoup selon les dépôts. La provenance du nitrate est discutée. Les sources possibles sont des aérosols marins, l’érosion des roches des Andes ou le lessivage des matières fécales telles que le guano (la source traditionnelle du salpêtre en Europe). Quelle que soit son origine, il semble que le nitrate de sodium ait été concentré par des cycles de dissolution puis de re-déposition d’une croûte solide menant à un enrichissement en nitrate. Les dépôts se trouvent dans une bande longue de quelques centaines de kilomètres et parallèle à la Cordillère de la Côte (en vert sur la carte à gauche, source CIA).
Le nitrate de sodium est une bonne source d’azote pour l’agriculture, donc un engrais, et peut aussi être transformé en acide nitrique pour la préparation d’explosifs. Même si la première cargaison envoyée en Europe a dû être jetée à la mer faute d’acheteur, le nitrate de sodium, sous le nom de salpêtre du Chili, a rapidement trouvé un marché et l’exportation du salpêtre du Chili est devenue un contributeur important à l’économie. En 1890 les droits de douane sur le salpêtre représentaient 50% du revenu du gouvernement Chilien. La technologie a été progressivement améliorée, notamment grâce aux contributions du chimiste Pedro Gamboni qui a remplacé l’ancienne méthode d’extraction du nitrate, qui consistait à chauffer du caliche avec l’eau dans de grandes cuves, par une extraction utilisant la vapeur, à la fois plus efficace et plus économe en combustible. Gamboni a également mis en évidence la présence d’iode (sous forme d’iodate de sodium) dans le caliche et a mis au point une méthode d’extraction. Le Chili est aujourd’hui le premier producteur mondial d’iode. Plus tard Gamboni a aussi su extraire le borate du caliche.
La guerre du Pacifique
L’importance croissante du salpêtre de Chili dans l’économie a fini par provoquer des différends. Malgré son nom, une bonne partie des gisements du salpêtre du Chili se trouvait en Bolivie et au Pérou. Si les terres étaient boliviennes, l’exploitation des gisements était le fait d’entreprises chiliennes. Ces dernières payaient une licence à la Bolivie mais la Bolivie souhaitait en tirer davantage. En 1879 la Bolivie chercha à augmenter ses revenus et
les Chiliens se sont révoltés et ont  pris les armes. Selon un traité secret entre la Bolivie et le Pérou, ce dernier se joignait à la Bolivie pour combattre les Chiliens et la guerre du Pacifique commença. Si la Bolivie et le Pérou étaient en supériorité numérique, les Chiliens avaient l’avantage qualitatif. En 1883 le Pérou signait le traité d’Ancon selon lequel la province de Tarapaca est cédée au Chili qui en plus assume l’administration des provinces d’Arica et de Tacna. Cette administration se poursuit jusqu’en 1929 quand la région de Tacna retourne au Pérou et celle d’Arica est attaché au Chili. La paix entre le Chili et la Bolivie n’est signée qu’en 1904 (l’agréablement nommé ‘traité de paix, d’amitié et de commerce’), mais la Bolivie n’a jamais accepté la perte de la province d’Antofagasta qui lui donnait accès à l’océan Pacifique. Le sujet était encore devant la Cour Internationale de la Justice en 2018.
pris les armes. Selon un traité secret entre la Bolivie et le Pérou, ce dernier se joignait à la Bolivie pour combattre les Chiliens et la guerre du Pacifique commença. Si la Bolivie et le Pérou étaient en supériorité numérique, les Chiliens avaient l’avantage qualitatif. En 1883 le Pérou signait le traité d’Ancon selon lequel la province de Tarapaca est cédée au Chili qui en plus assume l’administration des provinces d’Arica et de Tacna. Cette administration se poursuit jusqu’en 1929 quand la région de Tacna retourne au Pérou et celle d’Arica est attaché au Chili. La paix entre le Chili et la Bolivie n’est signée qu’en 1904 (l’agréablement nommé ‘traité de paix, d’amitié et de commerce’), mais la Bolivie n’a jamais accepté la perte de la province d’Antofagasta qui lui donnait accès à l’océan Pacifique. Le sujet était encore devant la Cour Internationale de la Justice en 2018.
A gauche : Déplacement des frontières à la suite de la Guerre du Pacifique. Source US Library of Congress.
La chute
En 1913 les chimistes allemands Fritz Haber et Carl Bosch ont mis au point une synthèse industrielle de l’ammoniac à partir de l’azote de l’air et de l’hydrogène. L’ammoniac est facilement transformé en acide nitrique, mettant ainsi fin au quasi-monopole du salpêtre du Chili. Ce procédé était vital pour l’Allemagne pendant la Première Guerre Mondiale pour permettre la synthèse des explosifs (l’Allemagne ne pouvant plus se fournir au Chili en raison du blocus naval) et son importance n’a cessé de grandir depuis. Aujourd’hui la production annuelle d’ammoniac par le processus Haber-Bosch est de l’ordre de 240 millions de tonnes par an, comparable à la quantité d’azote atmosphérique fixée par la biosphère, et l’ammoniac est la molécule de synthèse produite en plus grande quantité au monde, heureusement davantage pour les engrais que pour les explosifs. Cette évolution n’a pas manqué de peser sur le Chili et ses exportations de salpêtre sont en constante diminution. Des villes minières du désert d’Atacama comme Humberstone sont devenus des villes fantômes.
Un nouveau départ.
Si le marché du salpêtre n’a pas totalement disparu (curieusement, il est admis comme engrais pour l’agriculture organique aux Etats-Unis, mais pas ailleurs, le nitrate provenant du processus Haber Bosch est interdit partout), ce n’est plus la locomotive économique de la fin du 19ème siècle. Toutefois, l’invention de la batterie au lithium à la fin du 20ème siècle a généré un marché pour cet élément jusqu’ici peu recherché. Le lithium a deux sources principales : des roches cristallines et les déserts salés ou salars. Des sels de lithium sont lessivés des roches volcaniques de Andes, et dans ces régions désertiques où l’insolation est forte et la pluviométrie faible, les eaux s’évaporent et des dépôts d’évaporites sont formés donnant des déserts salés ou salars. Les salars du Chili, de la Bolivie et de l’Argentine contiennent des quantités importantes de lithium estimées à 50% des réserves mondiales. Malheureusement, les sels de lithium ne sont qu’une très faible partie des évaporites. Il n’y a pas de processus de concentration sélective comme nous l’avons vu pour le nitrate de sodium.

Salar d’Uyuni (Bolivie). Photo: Sonia Iodice
Le chlorure de sodium (ou sel commun) est de loin le sel le plus important mais il y a aussi des sels (en général des chlorures) de potassium, de magnésium et du lithium. Lors de l’évaporation des eaux de pluie, c’est surtout le très abondant chlorure de sodium qui cristallise le premier. Les sels de magnésium, potassium et lithium, beaucoup moins concentrés et plus solubles, restent en solution dans l’eau. Un salar se présente donc comme une croûte solide de chlorure de sodium sous laquelle se trouve une solution de sels. Pour l’extraction du lithium, il faut donc séparer l’aiguille du chlorure de lithium de la botte de foin des autres sels présents. On extrait le liquide sous la croûte solide, puis celui-ci est laissé dans de grands pans pour permettre une évaporation partielle après quoi, si tout va bien, une bonne partie du chlorure de sodium sera précipitée et le liquide surnageant sera enrichi en lithium. Ce liquide, en principe plus riche en lithium, est alors soumis à une ou plusieurs étapes de concentration avant de pouvoir obtenir un produit pur. Le processus est lent, consomme beaucoup d’eau (jamais idéal dans un désert) et produit de grands volumes de sels indésirables comme produits secondaires. De nombreux laboratoires travaillent actuellement à la recherche de méthodes plus efficaces d’extraction du lithium.
En conclusion, nous avons vu que les régions inhospitalières telles que le désert d’Atacama peuvent néanmoins être la source de matériaux forts utiles.
2 réflexions sur « Les richesses du désert »
fort intéressant, merci du partage
Informations très intéressantes.
Merci !